2023年6月14日,达石药业发布新闻稿称,其与中科院上海药物研究所(简称上药所)联合研发的抗体偶联药物(ADC)DS001分子获得中国国家药监局药品审评中心(CDE)临床试验默示许可,针对适应症为多种晚期恶性肿瘤。
DS001是一款创新ADC分子,它采用了达石药业专有的VK连接子技术,解决了传统ADC分子无法携带多个脂溶性小分子弹头的问题,显著地提高了ADC分子对肿瘤组织的穿透力。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
在临床前研究中,DS001显示了良好的肿瘤抑制效果和安全性,预计能在难治性恶性实体肿瘤如胰腺癌和胃癌的治疗上显示出一定疗效优势,以满足晚期肿瘤病人的重大临床需求。据达石药业新闻稿介绍,DS001的筛选工作由上药所生物技术药物研发中心王春河课题组完成,然后转化到达石药业,由后者的项目团队完成了该分子的上下游工艺开发、中试生产、质量研究、制剂研究和临床前的药效、代谢和安全性评价和临床批件申报工作。该项目后续的临床开发将由达石药业负责推进,并独占该分子100%的开发及商业权益,上药所将获得里程碑付款及后续销售提成。
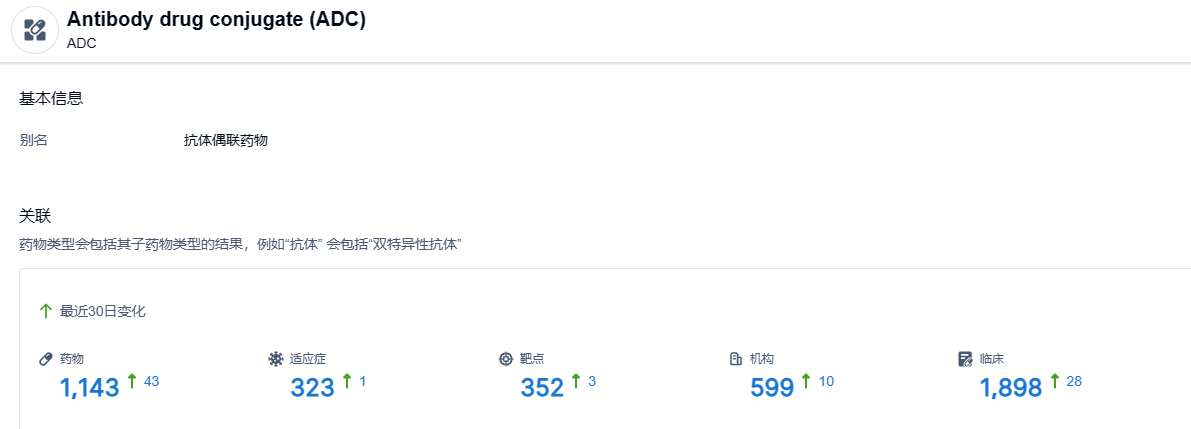
根据智慧芽新药情报库所披露的信息,截止到 2023 年6月16日,ADC这一药物类型共有在研药物1143个,包含的适应症有323种,靶点352个,在研机构599家,涉及相关的临床试验1898件。。。ADC药物等是目前研发热门的领域之一,此次DS001获批临床,再次给ADC的研发热度新增了一把火。