2023年6月20日,辉瑞(Pfizer)宣布,美国FDA已批准口服PARP抑制剂Talzenna(他拉唑帕利,talazoparib)联合Xtandi(恩扎卢胺,enzalutamide)用于同源重组修复(HRR)基因变异的转移性去势抵抗性前列腺癌(mCRPC)成人患者的治疗。
Talzenna(Talazoparib)由辉瑞公司研发,是一种聚ADP-核糖聚合酶(PARP)抑制剂。临床前研究表明,Talazoparib高度有效,具有双重作用机制,可以通过阻断PARP酶活性以及将PARP捕获在DNA损伤位点上来诱导肿瘤细胞死亡。2018年10月美国FDA批准他拉唑帕尼用于治疗携带有害或怀疑有害的生殖系BRCA突变、HER2阴性的局部晚期或转移性乳腺癌患者。恩扎卢胺为雄激素受体抑制剂,是治疗mCRPC、非转移性去势抵抗性前列腺癌、转移性去势敏感性前列腺癌的标准疗法。两款药物的联合疗法将对前列腺癌患者将实现1+1大于2的作用,为患者带来更优效的治疗选择。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
临床试验数据显示,组合疗法可将HRR基因突变mCRPC患者的疾病进展或死亡风险降低55%。辉瑞在新闻稿中表示,Talzenna是首个获批与现有标准治疗(恩扎卢胺)联合用于HRR基因突变mCRPC成人患者的PARP抑制剂。
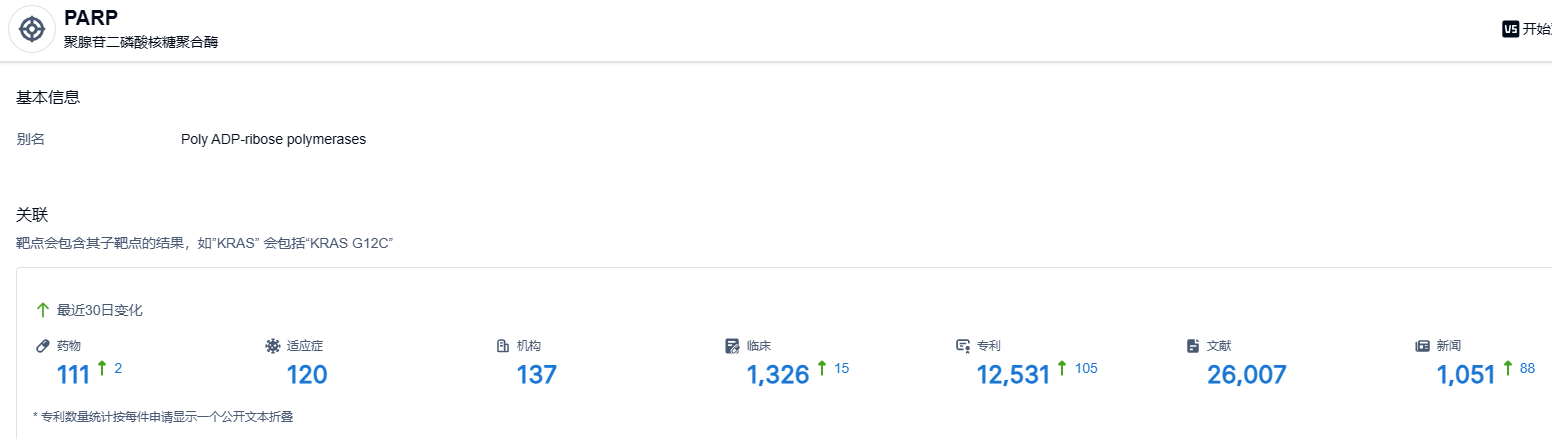
根据智慧芽新药情报库所披露的信息,截止到 2023 年6月22日,PARP 靶点共有在研药物111个,包含的适应症有120种,在研机构137家,涉及相关的临床试验1326件,专利多达12531件……PARP靶点是众多药企布局的重点,国内药企中恒瑞医药、百济神州均有该靶点新药成功上市,期待更多药企在该靶点中的表现。