2023年7月10日,清普生物发布新闻稿称,美国FDA完成对该公司首个项目QP001新药上市申请(NDA)的立卷审查,并发出关于QP001项目NDA的正式受理函,标志着QP001项目的NDA进入实质审查阶段。PDUFA日期为2024年2月26日。
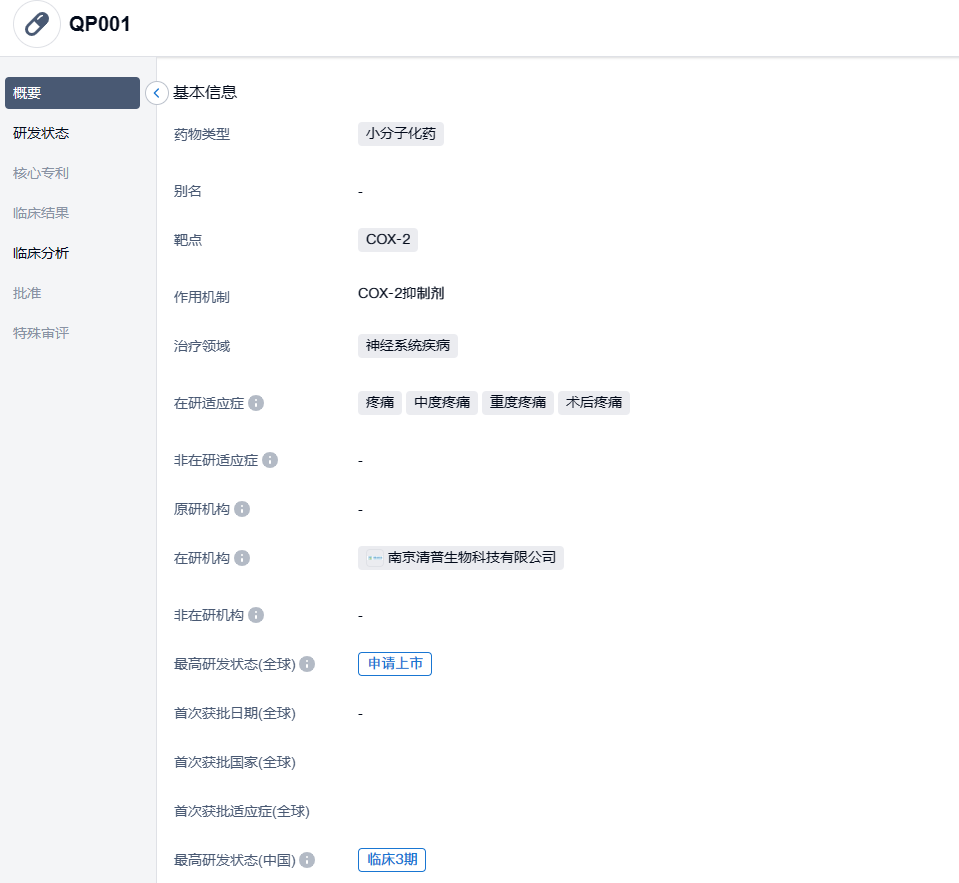
QP001注射液是清普生物系列非阿片类镇痛新药管线的首款产品,中美双报,可用于治疗各类急性疼痛,尤其适用于围术期镇痛,相比现有同类药物在镇痛强度、安全性和镇痛维持时间上均有显著优势。QP001项目基于清普自主知识产权的难溶药物增溶技术平台(SimSolTM)开发。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
此前,清普生物已同FDA顺利召开关于QP001项目的pre-NDA会议,达成多项共识,并收到FDA关于QP001项目的“Application Fee Waivers”(注册费用减免)确认函。根据美国《联邦食品、药品和化妆品法案》(FD&C Act)第736(d)(1)(C)章,南京清普生物可享受QP001项目NDA注册费用部分减免的优惠,成为国内极少数获得FDA“Application Fee Waivers”(注册费用减免)的生物医药公司之一。
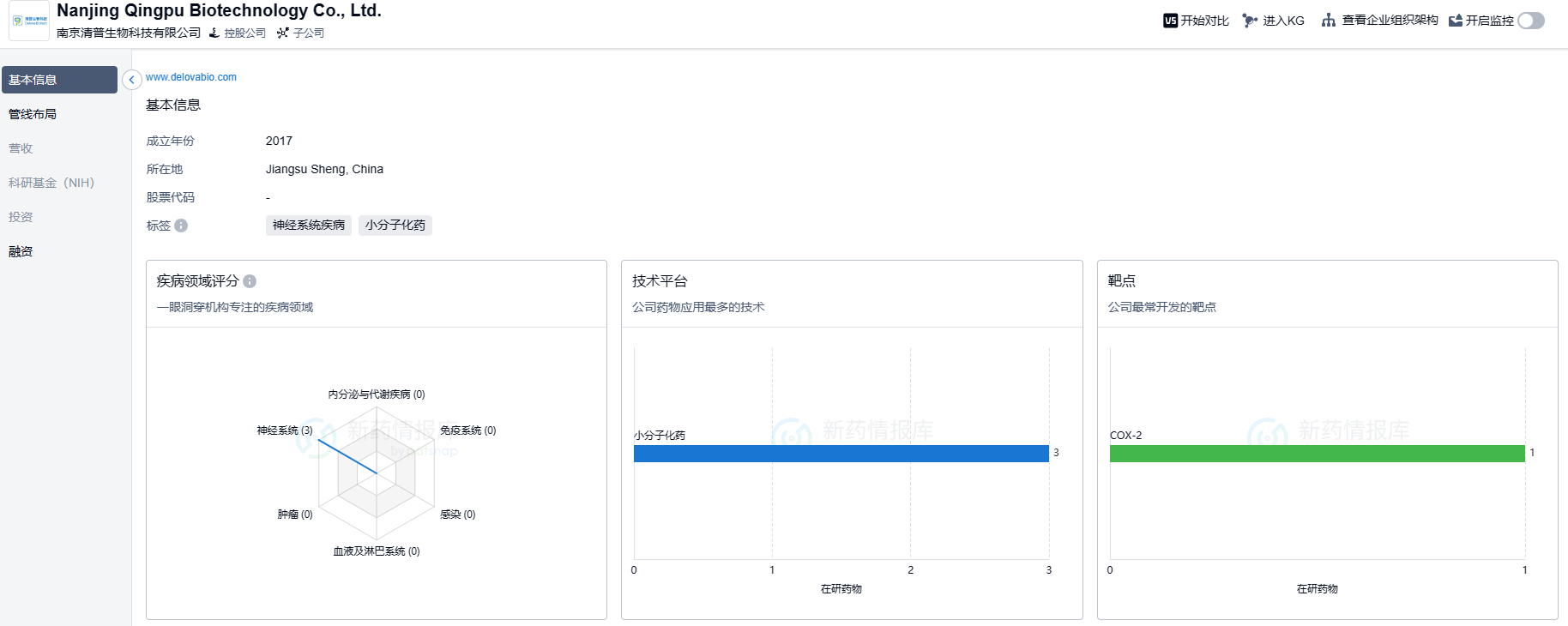
根据智慧芽新药情报库所披露的信息,截止到 2023 年7月12日,南京清普生物科技有限公司在小分子新药有非常大的投入,研发重心在神经系统领域,期待该公司核心产品QP001能够早日在国内外上市。