2023年8月24日,康方生物旗下PD-1/VEGF双特异性抗体药物-依沃西单抗(AK112)已参与国家药监局药品审评中心(CDE)的优先审评。依沃西单抗主要用于治疗联合培美曲塞和卡铂用于经EGFR酪氨酸激酶抑制剂(EGFR-TKI)治疗后进展的EGFR突变的局部晚期或转移性非鳞非小细胞肺癌(NSCLC)。
依沃西单抗是康方生物自主研发的,利用其独特的Tetrabody技术设计,能够阻止PD-1与PD-L1和PD-L2的结合,同时阻止VEGF与其受体的结合。其阻断效果可能比联合使用两种药物更加有效。在2022年12月6日,康方生物与Summit达成了合作协议,后者支付了50亿美金的总费用(其中5亿美金首付款)以获得依沃西单抗在美国、加拿大、欧洲和日本的开发和商业化权益。此外,康方生物仍保留其他地区的开发和商业化权益。依沃西单抗已于2023年8月1日向中国国家药品监督管理局药品审评中心(CDE)提交上市申请,并已被受理,预计在2024年获批。目前,该药物已3次入选CDE的突破性治疗品种,包括最新的上市申请。
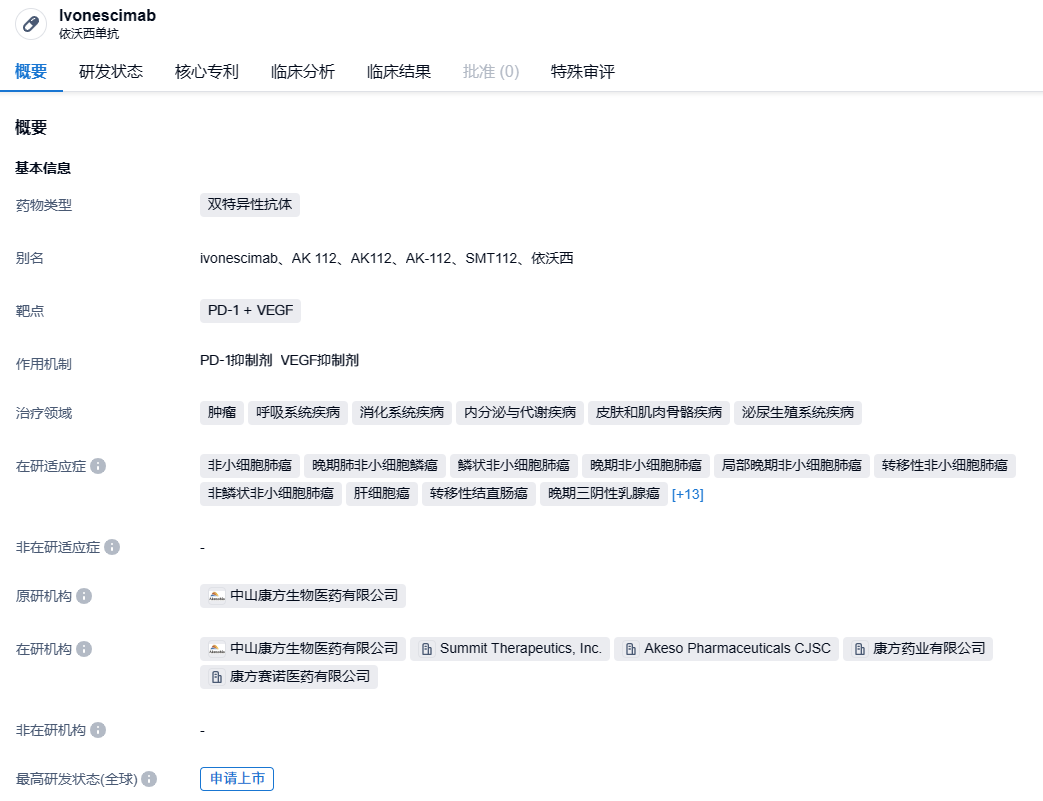 (文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
PD-1抗体和VEGF阻滞剂的结合治疗方案已在多种癌症(包括非小细胞肺癌、肾细胞癌和肝细胞癌)的治疗中展现出强大抗癌效果。例如,在2022年的美国临床肿瘤学会(ASCO)年会上,康方生物公布了其进行的二期临床试验结果,该试验使用依沃西单抗联合化疗治疗EGFR-TKI治疗失效的EGFR突变型晚期非鳞状NSCLC。数据显示:这种疗法带来的客观缓解率(ORR)高达68.4%,疾病控制率(DCR)达94.7%,中位无进展生存期(PFS)为8.2个月,而6个月的无进展生存率为69.3%。
目前,依沃西单抗用于治疗NSCLC正在全球范围内进行三期临床试验,并包含了中国、美国和欧洲等发达国家,将其与标准疗法PD-(L)1抑制剂结合进行治疗。例如,2023年6月12日,Summit Therapeutic在clinicaltrials.gov网站上登记了一项研究,该研究对比了Ivonescimab(依沃西单抗,PD-1/VEGF双抗)联合化疗与Pembrolizumab(K药,帕博利珠单抗)联合化疗对于一线治疗转移性鳞状非小细胞肺癌的研究(HARMONi-3,NCT05899608)。然后在同年的8月18日,康方生物宣传其自主研发的双特异性抗体新药依沃西单抗(AK112,PD-1/VEGF 双抗)联合化疗对比替雷利珠单抗联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌(sq-NSCLC)的注册性 III 期临床试验已经完成首例患者给药。
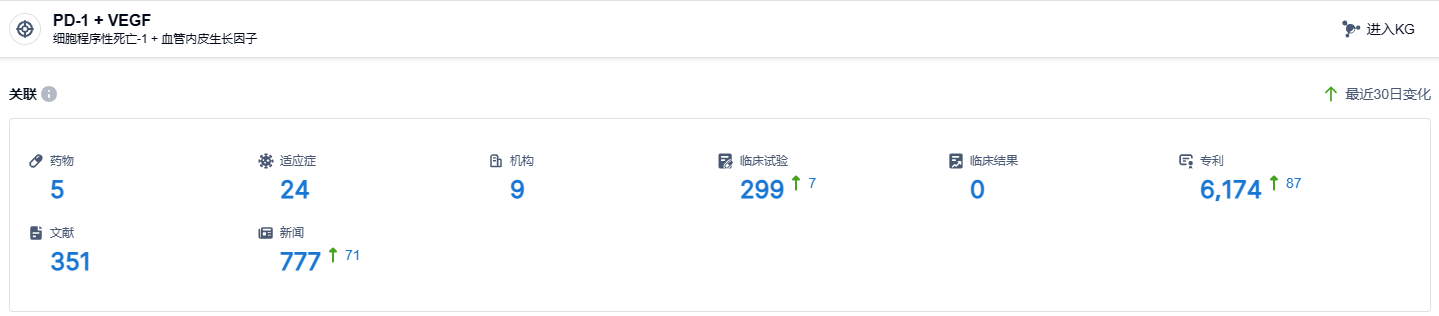
根据智慧芽新药情报库所披露的信息,截止2023年8月25日,全球 PD-1/VEGF 靶点新药共有5个在研,共有24种适应症,涉及9家研发机构,及299个相关临床试验。依沃西单抗预期将为超过 220 万新发肺癌病人,其中超过 81 万中国患者,提供新的治疗机会。