2023年9月22日,中国国家药监局(NMPA)的官网上公开了最新的信息:复宏汉霖公司开发的抗PD-1单抗斯鲁利单抗注射液的新适用病症上市申清已被批准。这是该产品在中国市场中得到批准的第四个适应症,其适应疾病为:使用化疗一线治疗局部晚期/复发或转移性食管鳞状细胞癌(ESCC)。
斯鲁利单抗是复宏汉霖公司自主研发的抗PD-1单抗。在2022年3月24日,由上海复宏汉霖生物技术股份有限公司自主开发的创新型PD-1抑制剂斯鲁利单抗(HLX10,商品名为:汉斯状®)被中国国家药监局(NMPA)批准上市,用于治疗在成人晚期实体瘤经治患者中无法切除或转移性的微卫星高度不稳定(MSI-H)。此前,该药在中国已经被批准用于治疗三个适应病症,包括微卫星高度不稳定(MSI-H)实体瘤、鳞状非小细胞肺癌(sqNSCLC)以及广泛期小细胞肺癌(ES-SCLC)。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
该新增适应病症上市申请主要基于一项名为ASTRUM-007的随机、双盲、多中心、3期临床试验。这项试验由中国医学科学院肿瘤医院的黄镜教授主要研究,对比了斯鲁利单抗联合化疗或安慰剂联合化疗一线治疗局部晚期/复发或转移性ESCC的效果和安全性。这项研究的结果已经在2022年中国临床肿瘤学会(CSCO)年会和欧洲肿瘤内科学会亚洲年会(ESMO Asia)上进行了口头报告,并且在2023年2月发表于《自然-医学》(Nature Medicine)。这项试验包括了551例以前未接受治疗、PD-L1阳性(综合阳性评分≥1)的晚期ESCC患者。数据表明,斯鲁利单抗联合化疗组的中位无进展生存期(PFS)和中位总生存期(OS)分别达到5.8个月和15.3个月,明显优于安慰剂联合化疗组的(5.3个月和11.8个月)。研究中斯鲁利单抗联合化疗的安全性良好,没有发现新的安全性信号。
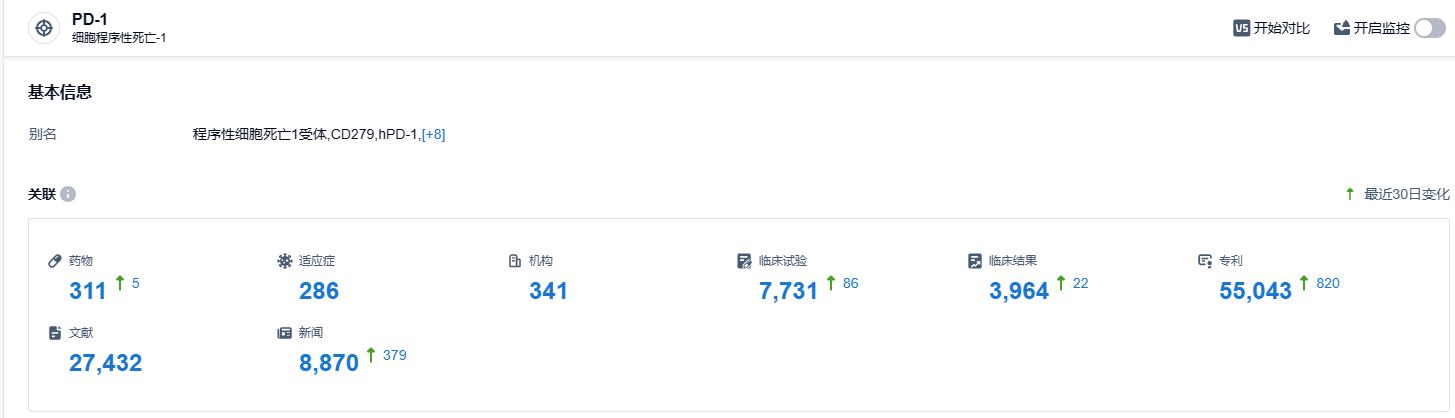
根据智慧芽新药情报库所披露的信息,直至2023年8月23日,PD-1靶点共有在研药物311个,适应病症有286种,在研机构341家,涉及相关的临床试验7731件,专利达到55043件……PD-1/PD-L1靶点是一个研发非常火热的领域,国内目前已经有超过10种相关新药上市,例如恒瑞的卡瑞利珠单抗年销售额峰值甚至近50亿元人民币。在这个竞争激烈的市场,商业化以及进一步的临床推进成为了药企争夺的关键,我们期待斯鲁利单抗能在竞争中崭露头角。