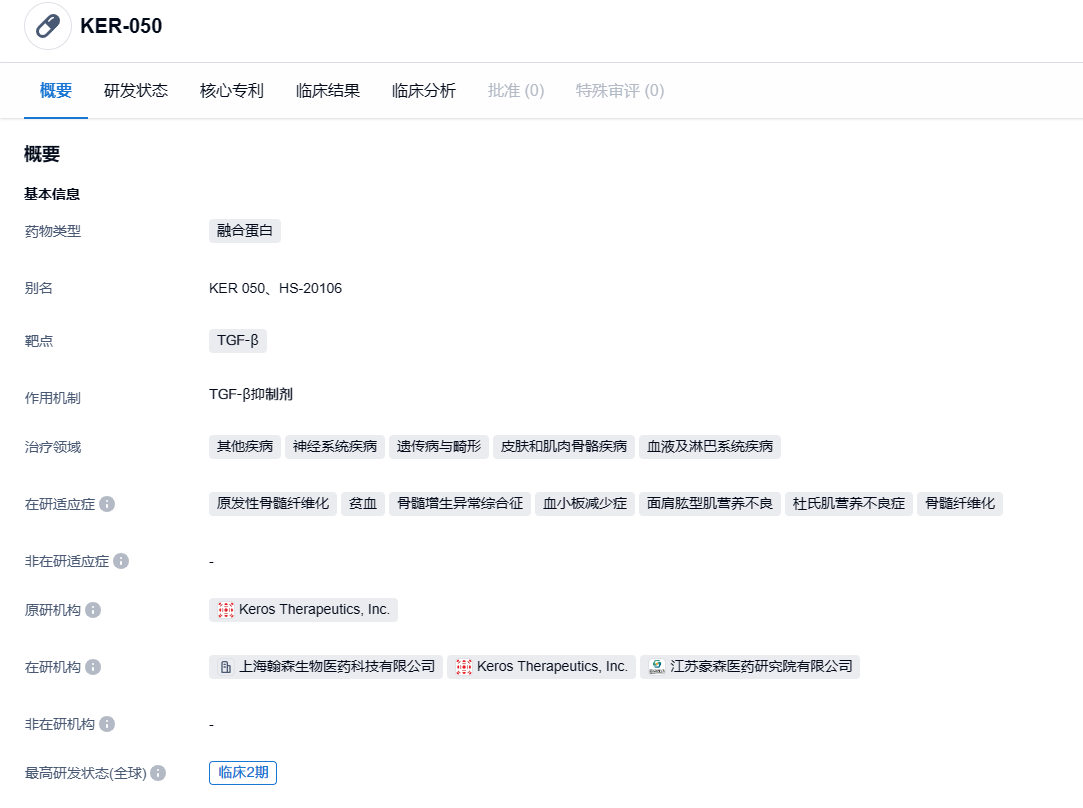
2023年10月18日,中国国家药监局药品审评中心(CDE)的官方网站公告,Keros Therapeutics所提交的一款一类新药HS-20106注射液已获取临床试验默示许可,此药物的研发主要针对各种不同原因引发的血细胞减少症。
Keros Therapeutics正在开发的主打药物HS-20106(KER-050)是一款“工程化配体捕获体”,由经过改造的TGF-β受体(即激活素受体IIA型)配体结合域与人源抗体的Fc区域融合而成。此次,KER-050正处于临床二期的开发阶段,主要针对骨髓增生异常综合征(MDS)以及骨髓纤维化患者的血细胞减少(含贫血及血小板减少)的治疗。2021年12月,翰森制药和Keros Therapeutics联合发布消息,双方已就后者主要药物KERO-050在华独家权益达成战略联盟。合作协议约定,翰森制药将获得KERO-050在中国大陆、香港及澳门地区的开发、生产及商业化的独家权益,为此,Keros公司将得到预付金2000万美元,同时有可能获得开发和商业里程碑付款高达1.705亿美元,以及产品净销售量的分级特许权使用费。2023年7月26日,据中国国家药监局药品审评中心(CDE)官网,Keros Therapeutics 与翰森制药附属公司翰森生物共同提交了关于一类新药HS-20106(KER-050)注射液的临床试验申请。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
根据ClinicalTrials网站,KER-050目前正在开展针对骨髓增生异常综合征(MDS)及骨髓纤维化(MF)患者的治疗研究,相关的临床试验已进展至二期临床。2021年12月,Keros 在第63届美国血液学会(ASH)公布了关于KER-050用以治疗MDS的II期临床试验的最新数据信息(截止至2021年10月25日)。该研究是一项开放标记、剂量递增的II期临床试验,主要评估KER-050治疗极低、低及中度风险MDS患者的疗效。研究结果显示,KER-050能够显著改善红细胞再生和血小板再生。
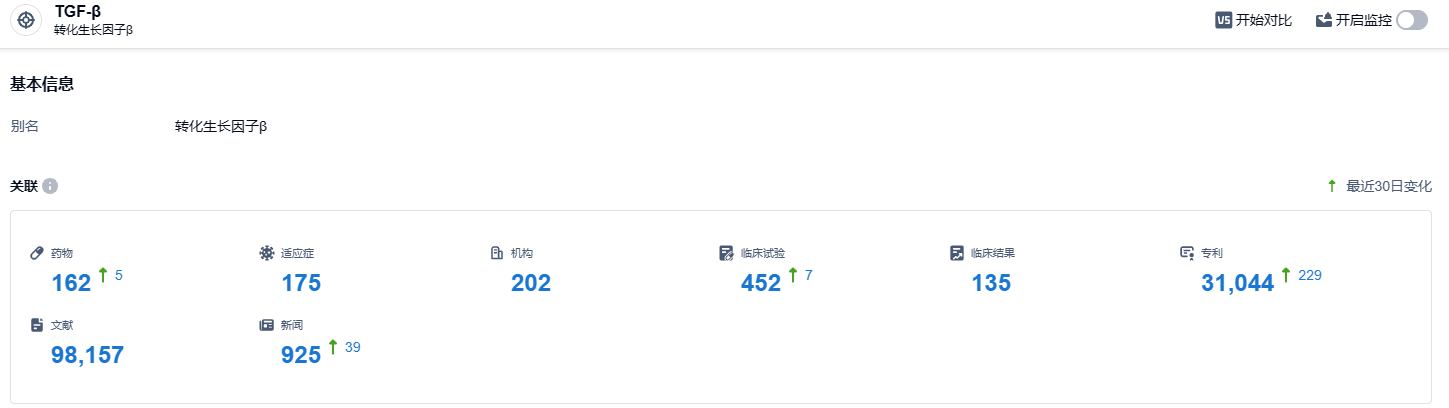
根据智慧芽新药情报库所披露的信息 ,截止2023年10月19日,TGF-β靶点的在研药物总数有162种,涵盖了175种适应症,开发机构数达202家,参与临床试验达452项,专利达到31044项。期待HS-20106(KER-050)未来的表现。