2023年11月27日,科伦博泰发布新闻稿称,其海外合作伙伴Ellipses Pharma引进的RET小分子激酶抑制剂KL590586(EP0031,简称A400),获得了美国FDA授予的孤儿药资格,用于治疗RET融合阳性实体瘤。
KL590586是新一代选择性RET抑制剂(SRI),对常见的RET基因融合和突变具有广泛活性,且具有克服第一代SRI耐药的潜力。在临床前研究中,KL590586在体外和体内对RET激酶表现出良好的抑制活性,在动物模型中也表现出良好的血脑屏障穿透性。目前,科伦博泰正在中国开展KL590586针对晚期RET阳性非小细胞肺癌的关键临床研究。2021年3月,科伦博泰将KL590586包括美国和欧洲在内的部分地区独家授权给Ellipses Pharma,科伦博泰保留大中华区、韩国、新加坡和马来西亚等部分亚太地区的权利。2022年6月,KL590586获得FDA批准的新药临床研究申请(IND),进行RET基因改变的恶性肿瘤患者的1/2期临床研究。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
2023年ASCO大会上报告了KL590586最新研究结果,KL590586在既往RET抑制剂耐药患者中显示出良好的抗肿瘤活性。在此报告了一项I/II期研究(KL400-I/II-01, NCT05265091)在RET改变的晚期肿瘤患者中的I期初步结果,以确定其安全性、药代动力学(PK)和疗效。截至2022年12月30日,研究纳入87例RET基因改变的晚期实体瘤患者,按研究设计分配到6个剂量组(10mg-120mg,QD)接受治疗。在该研究中,69例接受有效剂量(40mg-120mg)治疗的患者疗效可评估,其中57例为非小细胞肺癌(NSCLC),10例为甲状腺髓样癌(MTC),1例为胰腺癌,1例为卵巢癌。客观缓解率(ORR)为64%。截至数据截止日,绝大部分患者(58/69)仍在接受治疗,最长治疗时间超过11个月。在既往接受过系统治疗(中位线数为2,28%接受了抗PD-1/PD-L1治疗)的患者中,ORR为63%,疾病控制率(DCR)为91%,中位DOR未达到。其中9例接受第一代选择性RET抑制剂治疗后耐药的患者,7例肿瘤靶病灶缩小10%-69%,其中3例部分缓解(PR)、4例疾病稳定(SD)。在11例基线脑转移患者(既往未接受放疗)中,5例基线有可测量的脑部病灶,其中2例脑部病灶完全消失(100%),1例缩小80%,1例缩小47%。针对脑部病灶的DCR为100%。在既往未接受治疗的NSCLC患者中,ORR为76%,DCR为92%;4例为可测量脑部病灶患者(既往未接受放疗),3例脑部病灶响应为PR或CR。
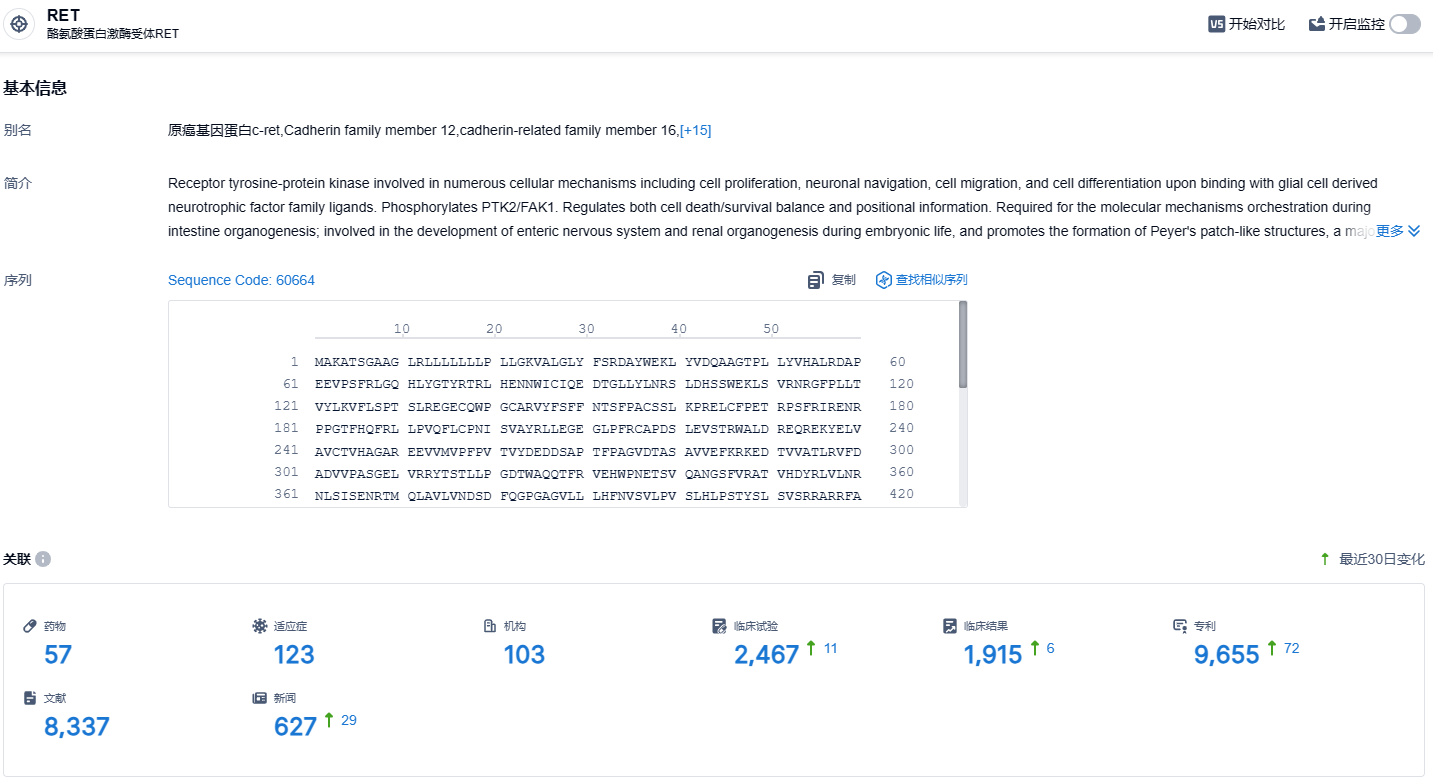
根据智慧芽新药情报库所披露的信息 (点击下方图片直达RET 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年11月28日,RET 靶点共有在研药物57个,包含的适应症有123种,在研机构103家,涉及相关的临床试验2467件,专利多达9655件……研究结果显示,KL590586在RET基因改变的肿瘤患者(包括第一代选择性RET抑制剂耐药和/或脑转移的NSCLC患者)中具有强大的临床活性,并且耐受性良好。期待KL590586的后续表现。