2023年11月28日,GSK宣布了3期临床试验DREAMM-7计划中的中期疗效分析的积极顶线结果。结果显示,抗体偶联药物belantamab mafodotin作为2线疗法,治疗复发或难治性多发性骨髓瘤达到了无进展生存期(PFS)的主要终点。
Blenrep(Belantamab mafodotin)是GSK开发的一种抗体偶联药物,由靶向B细胞成熟抗原(BCMA)的单克隆抗体与毒性载荷auristatin F通过不可切断的连接子连接而成。2020 年 8 月获 FDA 加速批准用于治疗先前经过四线治疗失败的多发性骨髓瘤(MM)患者。2022年 11 月,GSK 宣布基于确证性 III 期临床 DREAMM-3 研究的失败,已应美国 FDA 的要求,启动了撤销 Blenrep 美国上市许可的程序。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
DREAMM-7研究是一项随机、开放、多中心的III期临床,旨在评估belantamab mafodotin联合BorDex与达雷妥尤单抗联合BorDex治疗R/R MM患者的疗效和安全性,这些患者之前至少接受过一次治疗,并在最近一次治疗期间或之后出现疾病进展。研究共纳入494名受试者,按1:1的比例随机分组接受治疗。主要终点是PFS,关键次要终点包括OS、缓解持续时间和最小残留疾病阴性率。
结果显示,与 daratumumab+BorDex(硼替佐米+地塞米松)相比,Blenrep+BorDex 联用疗法可显著延长患者疾病进展或死亡时间。此外,还观察到显著且具有临床意义的 OS 趋势,目前试验仍在继续进行中,进一步监测 OS 结果。
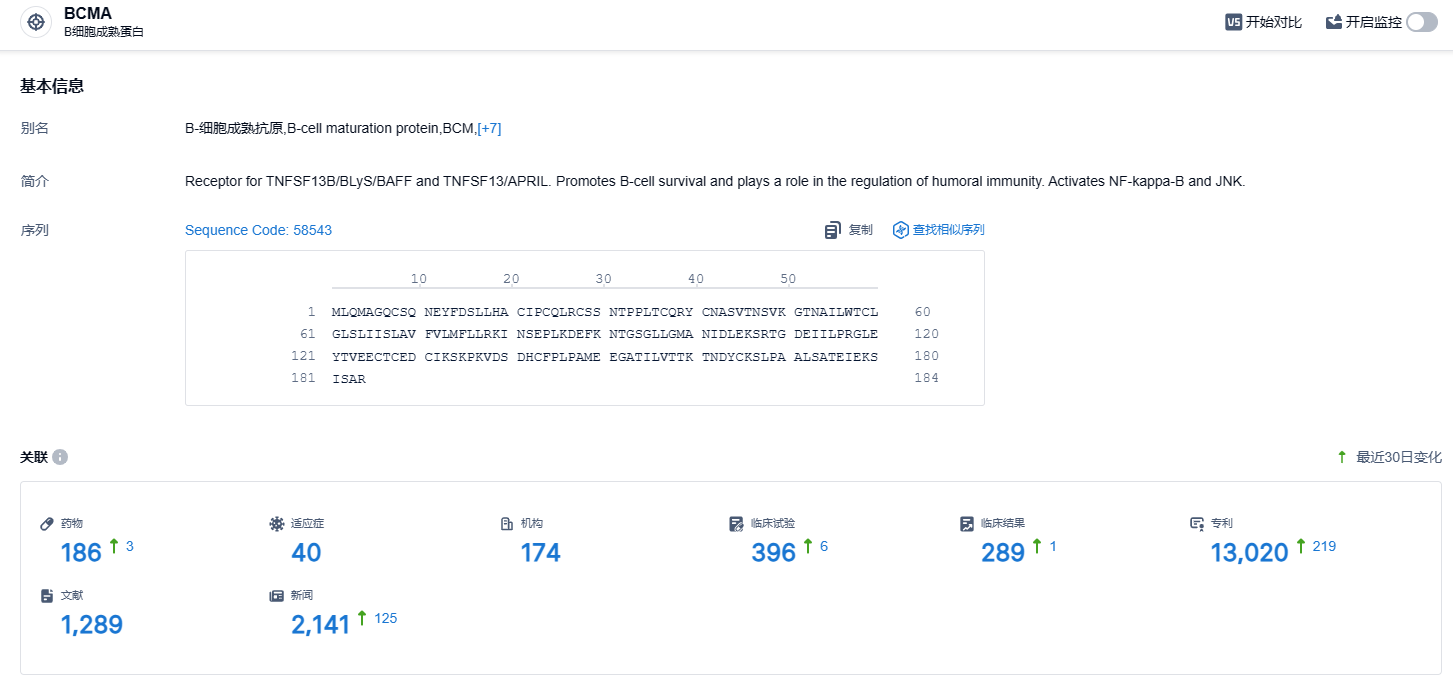
根据智慧芽新药情报库所披露的信息 (点击下方图片直达BCMA靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年11月29日,BCMA靶点共有在研药物186个,包含的适应症有40种,在研机构174家,涉及相关的临床试验396件,专利多达13020件……当前全球仅有 5 款 BCMA ADC 进入临床,且以海外药企布局为主。期待belantamab mafodotin能够再次上市。