2023年12月11日,科越医药(Kira Pharmaceuticals)宣布,该公司在2023年美国血液学协会(ASH)年会上,以口头报告的形式公布了双靶点补体抑制剂KP104在未接受补体抑制剂治疗的阵发性睡眠性血红蛋白尿症(PNH)患者中进行的临床2期试验的中期安全性和有效性数据。
KP104是一种具有独特作用机制的全球首创双功能补体生物药,靶向补体C5 + CFH。KP104旨在同时选择性抑制补体旁路和终端途径,提供一种强大的协同机制且可能更加有选择性的精准治疗补体介导的疾病。KP104还被设计成具有延长的半衰期和效力,其配方可用于静脉注射和皮下给药。KP104正进入多个适应症的2期临床试验,包括IgA肾病(IgAN)、C3肾小球病(C3G)、继发于系统性红斑狼疮的血栓性微血管病(SLE-TMA)和PNH。2期临床试验将在全球范围内进行,包括美国、中国、澳大利亚和韩国。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
阵发性睡眠性血红蛋白尿症(PNH)是一种罕见的危及生命的血液疾病,其特征是红细胞破坏、血栓形成和骨髓功能受损。PNH的患病人数在百万分之1-5,几乎都是由于基因突变导致产生异常造血干细胞引起。这些干细胞产生不规则的红细胞,这些红细胞很容易通过补体激活而被破坏。目前的治疗包括C5抑制剂,但无法解决与替代途径相关的血管外溶血(EVH)。或是C3抑制剂,可能解决EVH,但有存在不能充分阻断下游C5的问题,导致危及生命的突破性溶血(Breakthrough Hemolysis in PNH with Proximal or Terminal Complement Inhibition, N Engl J Med, July 14, 2022)。由于补体生物学的复杂性,结合多个靶点影响PNH病理学等种种因素,在疗效、安全性和给药便利性各方面都优于现有治疗手段的下一代药物的医疗需求仍然没有得到满足。
本次公布数据的是一项开放标签的2期临床试验,旨在评估KP104在既往未接受补体抑制剂的PNH患者中的疗效、安全性、耐受性、药代动力学(PK)和药效学(PD)。该2期研究的主要临床疗效评估指标包括乳酸脱氢酶(LDH)和血红蛋白(Hgb)水平、输血需求和FACIT-疲劳评分。对KP104的2期研究的中期分析显示,18名PNH患者完成了24/25周的三个递增剂量的治疗,并取得了积极的结果。
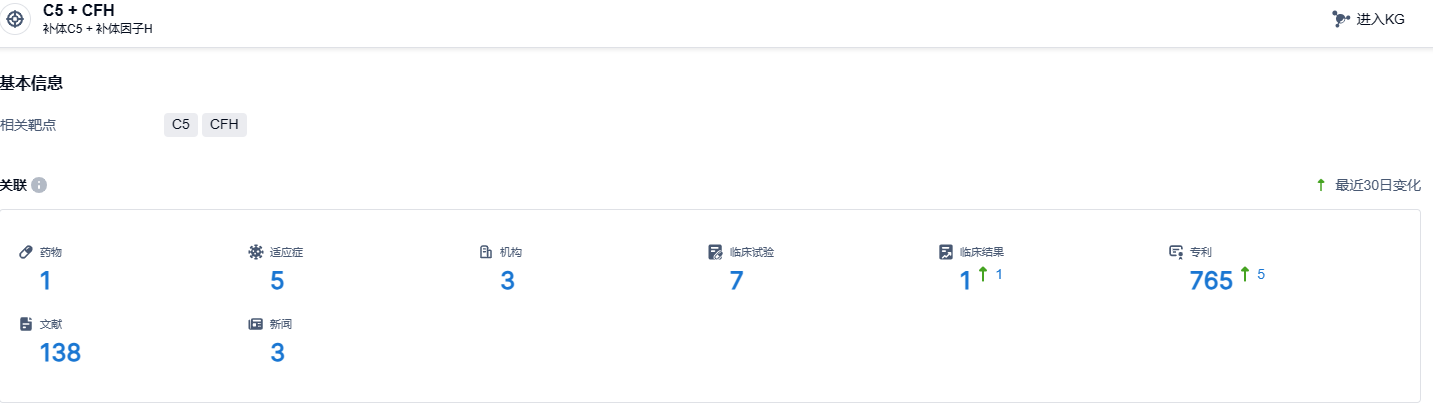
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达C5 + CFH靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年12月13日,C5 + CFH靶点共有在研药物1个,包含的适应症有5种,在研机构3家,涉及相关的临床试验7件,专利多达765件……补体蛋白C5是非常成功的一个补体药物靶点,首款药物Soliris 2020年销售额高达40.64亿美元,2022年销售额为37.62亿美元。第二款药物Ultomiris 2022年销售额高达19.65亿美元,今年上半年其销售额达13.64亿美元。作为全球首创双功能补体生物药,KP104靶向补体C5 + CFH,有望在补体蛋白C5赛道中占据优势。