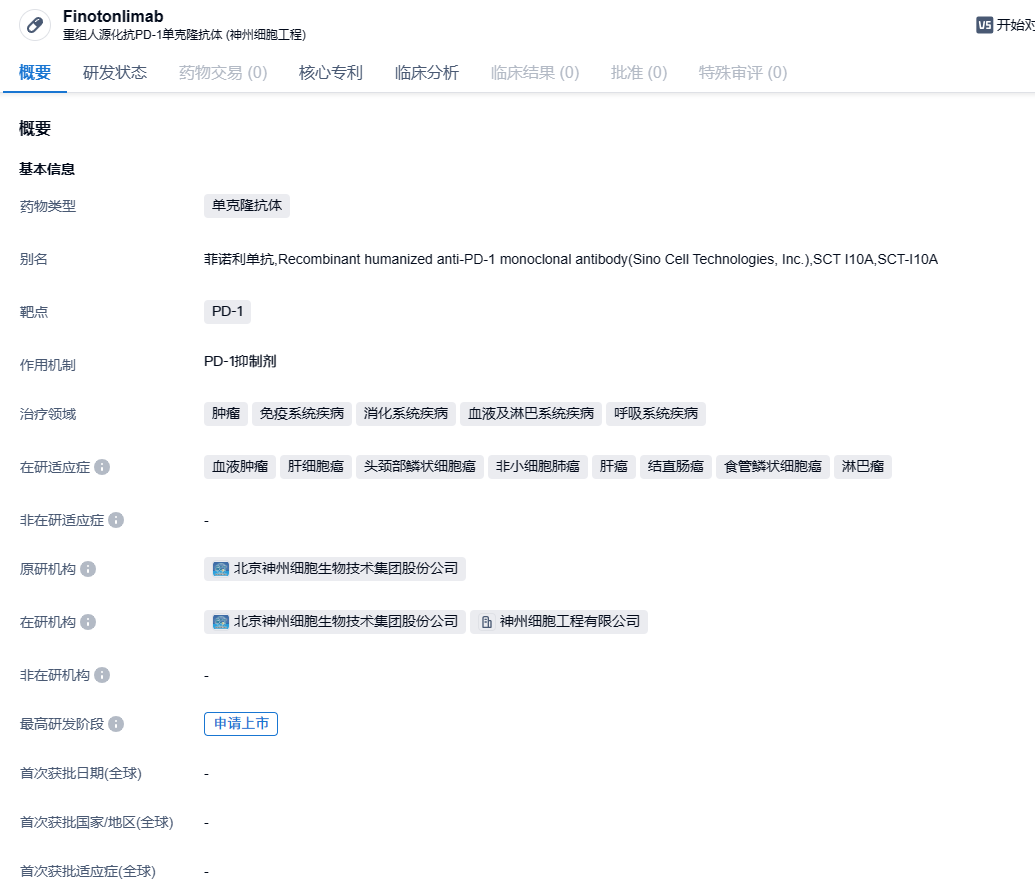
2024年1月17日,神州细胞宣布,该公司控股子公司神州细胞工程申报的菲诺利单抗注射液(SCT-I10A)联合贝伐珠单抗注射液(SCT510)用于治疗肝细胞癌新适应症的上市许可申请获中国国家药监局(NMPA)受理。本次SCT-I10A+SCT510联合疗法申报治疗对象为既往未接受过系统治疗的不可切除或转移性肝细胞癌患者。
菲诺利单抗是由神州细胞自主研发的一种重组人源化抗PD-1 IgG4型单克隆抗体注射液,此次申请的适应症为头颈部鳞状细胞癌。作为抗PD-1功能性单克隆抗体,菲诺利单抗通过阻断PD-1与其配体的结合,增加肿瘤部位的T细胞和炎性细胞因子的供给量,减少肿瘤微环境中调节性T细胞和髓系来源的抑制细胞的比例,从而改变肿瘤微环境,恢复和提高T细胞的免疫杀伤功能,以达到抑制肿瘤生长的效果。菲诺利单抗首个适应症头颈部鳞状细胞癌的上市申请已于2023年11月获得NMPA受理。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
菲诺利单抗计划用于治疗多种实体瘤,包括淋巴瘤、头颈鳞癌、食管鳞癌、结直肠癌、胃腺癌和鳞状非小细胞肺癌等。据中国药物临床试验登记与信息公示平台,该产品已进行多项临床试验,包括一线治疗复发性和/或转移性头颈部鳞状细胞癌的3期临床研究、一线治疗晚期肝细胞癌的2/3期试验、二线治疗晚期肺鳞癌的3期临床研究等。
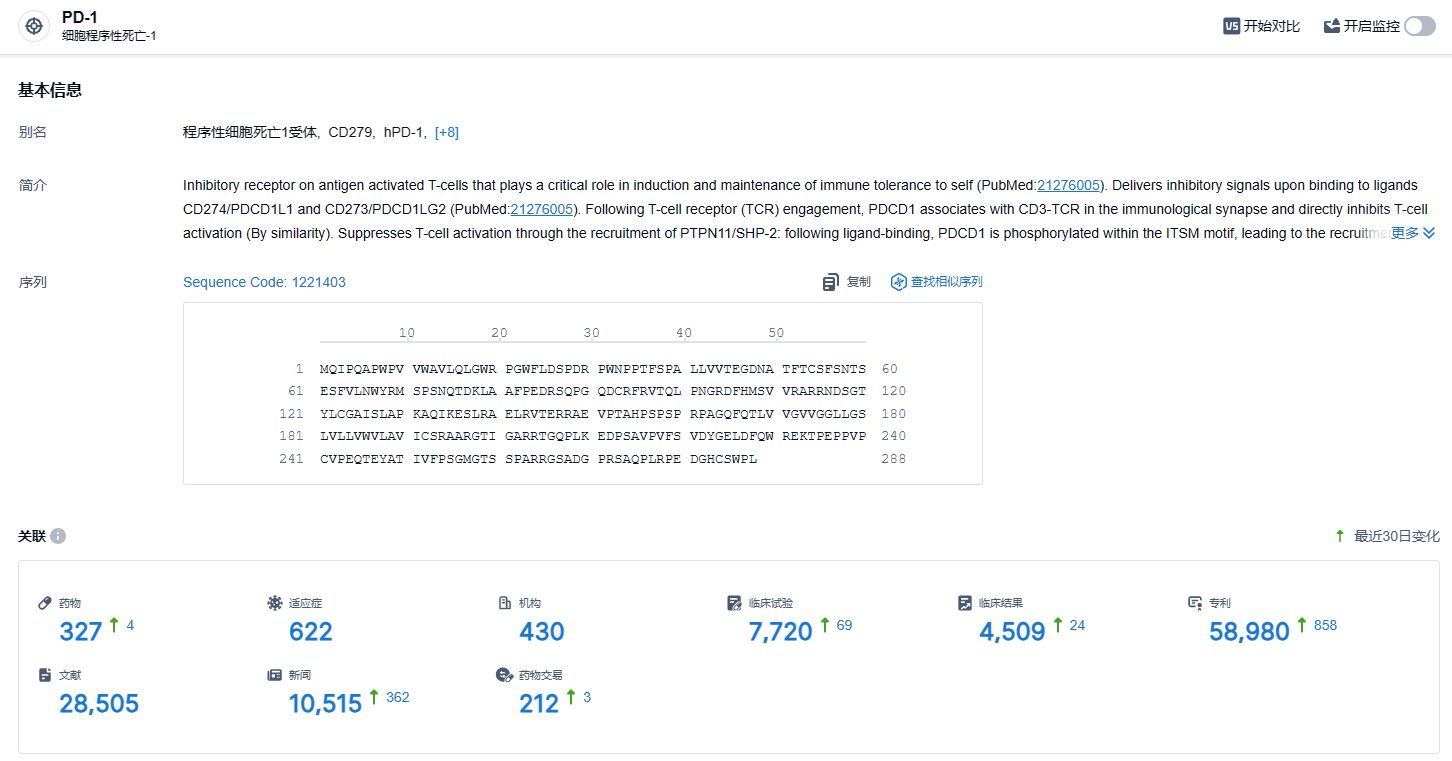
根据智慧芽新药情报库所披露的信息,截止到 2024 年1月19日,PD-1靶点共有在研药物327个,包含的适应症有622种,在研机构430家,涉及相关的临床试验7720件,专利多达58980件……截至目前,国内已获批上市多款抗 PD-1 和 PD-L1 单抗药物,即使 SCTI10A 顺利获批上市,其未来的市场销售仍将面临较为激烈的竞争态势,并同时受国家医保政策、市场环境变化、公司生产能力等多种因素影响,产品的商业化前景存在较大的不确定性。红海市场,竞争激烈。