2024年1月29日,阿斯利康和第一三共联合宣布,FDA已经接受Enhertu(德曲妥珠单抗)的补充生物制品许可申请(sBLA),用于治疗不可切除或转移性HER2表达实体瘤成人患者,这些患者既往接受过治疗或没有令人满意的替代治疗方案。此外,FDA还授予该sBLA优先审查资格。
德曲妥珠单抗(Trastuzumab deruxtecan)(研发代号:DS-8201)是一款抗体偶联药物(ADC),由抗HER2人源化单克隆抗体与载药拓扑异构酶Ⅰ抑制剂DXd(payload)通过可裂解连接子(linker)组成,其DAR值达理论最大值8,具有避免耐药、特异性强、高细胞毒性和安全性良好的特点。与HER2结合后,德曲妥珠单抗会破坏HER2信号,介导抗体依赖的细胞毒性反应,并通过内吞进入细胞内释放DXd,进而导致DNA损伤和细胞凋亡。此外,连接子与载药连接处的自切割修饰赋予的高效膜透过性,使德曲妥珠单抗能够发挥“旁观者效应”,克服瘤内异质性。本品最早由第一三共开发。2019年3月,阿斯利康与第一三共达成一项高达69亿美元的合作,在全球范围内共同开发和商业推广德曲妥珠单抗。2023年2月,注射用德曲妥珠单抗获得NMPA批准上市,单药适用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
该申请主要基于II期DESTINY-PanTumor02研究数据。这是一项全球性、多中心、开放标签、多队列的II期临床试验,旨在评估Enhertu(5.4mg/kg)在接受过治疗的局部晚期、不可切除或转移性的表达HER2的实体瘤患者中的疗效和安全性,包括胆道癌、膀胱癌、宫颈癌、子宫内膜癌、卵巢癌、胰腺癌或其他肿瘤。主要终点是由研究者评估确认的客观缓解率(ORR),次要终点包括缓解持续时间(DoR)、疾病控制率(DCR)、无进展生存期(PFS)、总生存期(OS)、安全性、耐受性和药代动力学。截至2023年06月08日,中位随访时间为12.75个月。结果显示,德曲妥珠单抗在既往接受过治疗的HER2表达的晚期实体瘤患者(n=267)总研究人群中经研究者评估的确认的ORR为37.1%(95% [CI]:31.3-43.2),中位DoR为11.3个月(95% CI:9.6-17.8),中位PFS为6.9个月(95% CI:5.6-8.0),中位OS为13.4个月(95% CI:11.9-15.5)。
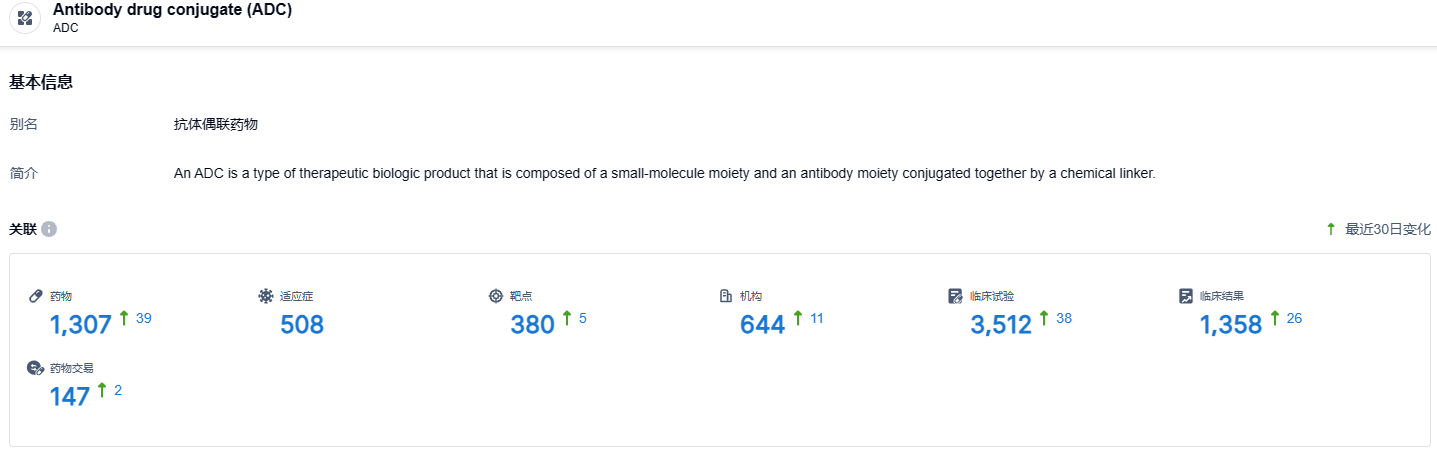
根据智慧芽新药情报库所披露的信息,截止到 2024年1月30日,ADC这一药物类型共有在研药物1307个,包含的适应症有508种,靶点380个,在研机构644家,涉及相关的临床试验3512件……ADC药物研发已成红海之势,而HER2更是布局更多的靶点之一。期待德曲妥珠单抗的后续表现。