日前,Iovance Biotherapeutics宣布,美国FDA已接受旗下细胞疗法lifileucel用于晚期黑色素瘤患者的生物制品许可申请(BLA),并授予其优先审评,PDUFA日期被设定为2023年11月25日。
今年3月,Iovance Biotherapeutics宣布,已经完成向美国食品和药物管理局(FDA)提交其肿瘤浸润淋巴细胞(TIL)疗法lifileucel(代号:LN-144)的滚动生物制品许可申请(BLA),以治疗那些在接受抗PD-1/L1治疗和靶向治疗期间或之后发生进展的晚期(不可切除或转移性)黑色素瘤患者。若本次顺利获批,lifileucel将成为全球首款治疗该类患者的TIL细胞疗法。此次获得优先审评,将有望缩短该疗法的上市进程。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
Lifileucel是基于患者自身的TIL细胞所研制的细胞疗法。TIL在癌症发生时会迁移到肿瘤处并且对肿瘤发起攻击。然而,通常患者体内的TIL数目不足以消灭肿瘤,而且肿瘤微环境会抑制TIL的功能。Iovance公司的TIL疗法从患者体内获取肿瘤组织并且提取TIL,然后在体外使用IL-2细胞因子刺激TIL的扩增,再将细胞注回患者体内,更有效地杀伤肿瘤细胞。与现有疗法相比,TIL技术的优点包括:①可以靶向多种肿瘤抗原;②能够实现一次性治疗;③由于TIL来源自体,因此不良反应少。Lifileucel目前已在包括黑色素瘤、宫颈癌、头颈部癌、肺癌实体瘤中显示出了疗效。
此次BLA递交上市申请,是基于在接受过抗PD-1治疗的晚期黑色素瘤患者中开展的C-144-01临床试验的数据支持。试验结果表明,一次性注射lifileucel,能够在接受过PD-1抑制剂和BRAF/MEK靶向疗法的难治性患者中,该疗法的疾病控制率达到了惊人的79.3%。且一次注射lifileucel,能够在接受过PD-1抑制剂和BRAF/MEK靶向疗法的难治性患者中,达到34.3%的总缓解率。
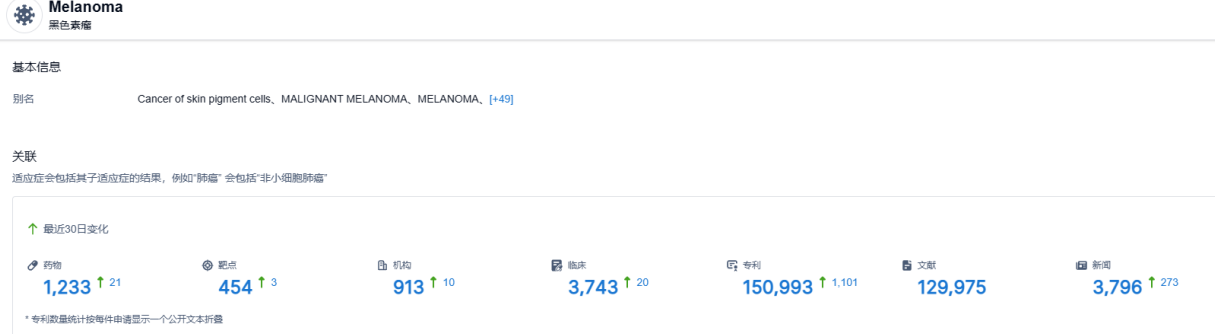
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 黑色素瘤 适应症注册登录后可免费获得该适应症下的在研药物、靶点、研发机构、临床试验等详细信息),黑色素瘤 适应症共有在研药物1233个,包含的靶点有454种,在研机构913家,涉及相关的临床试验3743件,专利多达150993件。。。lifileucel若本次顺利获批,将成为全球首款治疗该类患者的TIL细胞疗法。