2023年6月26日,中国国家药监局(NMPA)官网最新公示,复星凯特递交的阿基仑赛注射液新适应症上市申请已正式获批。根据中国国家药监局药品审评中心(CDE)优先审评公示,该产品此次获批适应症为:一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤(r/r LBCL)。
阿基仑赛注射液是一种自体免疫细胞注射剂,是复星凯特于2017年从吉利德科学(Gilead Sciences)旗下公司Kite Pharma引进Yescarta(Axicabtagene Ciloleucel)技术、并获授权在中国进行本地化生产的靶向CD19自体CAR-T细胞治疗产品。2021年6月,阿基仑赛在获得CDE批准上市,这是国内首个CAR-T细胞治疗产品。2021年6月至今,已有逾500位复发/难治性大B细胞淋巴瘤患者接受阿基仑赛的治疗。
(文中的所有图片均已设置链接,可直接点击图片跳转到新药情报库免费查看对应图片最新数据详细信息)
此次新适应症获批,是基于一项名为ZUMA-7的临床试验。ZUMA-7试验是一项全球性随机、开放标签的3期临床试验,共有359位原发难治或12个月内复发的LBCL成人患者入组,主要终点为无事件生存期(EFS),关键次要终点为客观缓解率(ORR)与总生存期(OS)。以往公布的试验结果显示,相比标准治疗组,Yescarta组患者的EFS显著延长(8.3个月 vs 2.0个月);Yescarta组独立审评委员会评估的ORR为83%,显著优于对照组的50%。
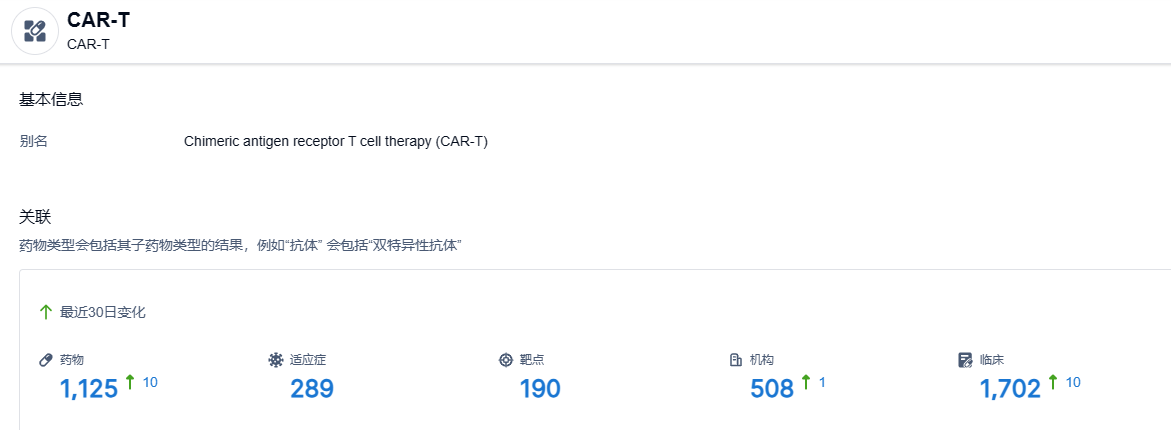
根据智慧芽新药情报库所披露的信息 ,截止到 2023 年6月28日,CAR-T这一药物类型共有在研药物1125个,包含的适应症有289种,靶点190个,在研机构508家,涉及相关的临床试验1702件……CAR-T等是目前研发热门的领域之一,期待更多国产新药的身影。